| Benzotriazol
|
![]()
|
| Más nevek |
1H-benzotriazol, 1,2,3-benzotriazol, BtaH
|
| Kémiai azonosítók
|
| CAS-szám |
95-14-7
|
| PubChem |
7220
|
| ChemSpider |
6950
|
|
|
| InChI |
|---|
| 1/C6H5N3/c1-2-4-6-5(3-1)7-9-8-6/h1-4H,(H,7,8,9) |
|
| InChIKey |
QRUDEWIWKLJBPS-UHFFFAOYSA-N
|
| ChEMBL |
84963
|
| Kémiai és fizikai tulajdonságok
|
| Kémiai képlet |
C6H5N3
|
| Moláris tömeg |
119,12 g/mol
|
| Megjelenés |
solid
|
| Sűrűség |
1,36 g/mL [1]
|
| Olvadáspont |
100 °C [2]
|
| Forráspont |
350 °C [2]
|
| Oldhatóság (vízben) |
20 g/L[2]
|
| Savasság (pKa) |
8,2[3][4]
|
| Lúgosság (pKb) |
< 0[4]
|
| Veszélyek
|
| R mondatok |
R20/22 R36 R52/53 [1]
|
| S mondatok |
–
|
| R/S mondatok |
–
|
| Rokon vegyületek
|
| Rokon vegyületek |
benzimidazol
|
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak.
|
A benzotriazol (BTA) nitrogéntatalmú heterociklusos aromás vegyület, képlete C6H5N3. Színtelen szilárd anyag.
Szerkezete
Molekulájában két kondenzált gyűrű található, az öttagú gyűrű A és B tautomer formájában létezhet, és ezeknek származékait – a C és D szerkezeteket – is elő lehet állítani.[5]

UV-, IR- és 1H-NMR spektroszkópiai vizsgálatok alapján szobahőmérsékleten túlnyomó részben az A izomer van jelen. Az 1-es és 2-es, valamint a 2-es és 3-as helyzetek közötti kötések tulajdonságai azonosak. A proton nem kötődik szorosan egyik nitrogénatomhoz sem, hanem inkább gyorsan vándorol az 1-es és 3-as atom között, ezért a molekula gyenge savként képes a proton leadására (pKa = 8,2)[3][4] vagy a nitrogénatom nemkötő elektronpárja révén nagyon gyenge bázisként protont is tud megkötni (pKa < 0).[4] Nemcsak savként vagy bázisként képes viselkedni, nemkötő elektronpárja révén más részecskékhez is tud kapcsolódni. Ennek révén például réz felületén stabil koordinációs vegyületet képez, így korróziógátló szerként hat.[5]
Előállítása
Egyik előállítási módja o-fenilén-diamin, nátrium-nitrit és ecetsav reakciója. Az átalakulás az egyik amincsoport diazotálásával megy végbe.[6]
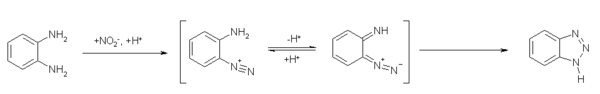
A szintézis javítható, ha alacsony hőmérsékleten (5–10 ˚C-on) hajtják végre, és rövid ideig ultrahangos fürdőt használnak.[7]
Környezeti hatások
A Rajna, illetve Elba folyók által az Északi-tengerbe mosódó, fagyálló, korróziógátló folyadékként használatos benzotriazol potenciálisan veszélyezteti a vízi élővilágot.[8]
Jegyzetek
- ↑ a b c chemdat.info Archiválva 2008. október 26-i dátummal a Wayback Machine-ben
- ↑ a b c SRC PhysProp Database: 1H-Benzotriazole Archiválva 2007. szeptember 27-i dátummal a Wayback Machine-ben
- ↑ a b Katritzky, A. R., Rachwal S.; Hitchings G. J. (1991. január 14.). „Benzotriazole: A novel synthetic auxiliary”. Tetrahedron (16-17), 2683–2732. o. DOI:10.1016/S0040-4020(01)87080-0.
- ↑ a b c d Katritzky, A. R.: Adventures with Benzotriazole. Lecture presented at various locations in 2002. Florida Center for Heterocyclic CompoundsFor. [2012. április 26-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. november 23.)
- ↑ a b Sease, Catherine (1978. május 1.). „Benzotriazole: A Review for Conservators”. Studies in Conservation 23 (2), 76–85. o. DOI:10.2307/1505798. JSTOR 1505798.
- ↑ Robert A. Smiley “Phenylene- and Toluenediamines” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a19_405
- ↑ Claudio, M. P. (2006. augusztus 29.). „Improved Synthesis of Benzotriazoles and 1-Acylbenzotriazoles by Ultrasound Irradiation”. Letters in Organic Chemistry 4 (31), 43–46. o. DOI:10.1002/chin.200731104. (Hozzáférés: 2011. november 23.) [halott link]
- ↑ Fagyálló az Északi-tengerben
Fordítás
Ez a szócikk részben vagy egészben a Benzotriazole című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.